COSA E' L'ACQUA PER INIETTABILI?
TIPI DI ACQUA E FARMACOPEE
Le acque farmaceutiche
Solo alcuni tipi di acqua farmaceutica hanno la designazione USP e sono oggetto di monografie ufficiali nell'attuale farmacopea US. Tuttavia, lo stesso documento afferma che "sebbene non esistano standard microbici assoluti per l'acqua (diverso è per quella destinata a diventare sterile), le norme cGMP richiedono che siano stabiliti e monitorati parametri appropriati". "(...) i.e. l'acqua utilizzata per la formulazione di un prodotto non deve contenere organismi in grado di crescere nel prodotto. (...)".
Per questo, in Bram-Cor, ogni sistema di trattamento dell’acqua è realmente personalizzato e orientato ad uno specifico impianto farmaceutico, linea e prodotto.
Il documento ISPE (ISPE BASELINE© GUIDE, Water and steam Systems) spiega quale acqua può essere utilizzata nello sviluppo, nella fabbricazione e nella preparazione di prodotti farmaceutici.
Queste acque rientrano in due categorie:
1. ACQUE COMPENDIALI
2. ACQUE NON COMPENDIALI
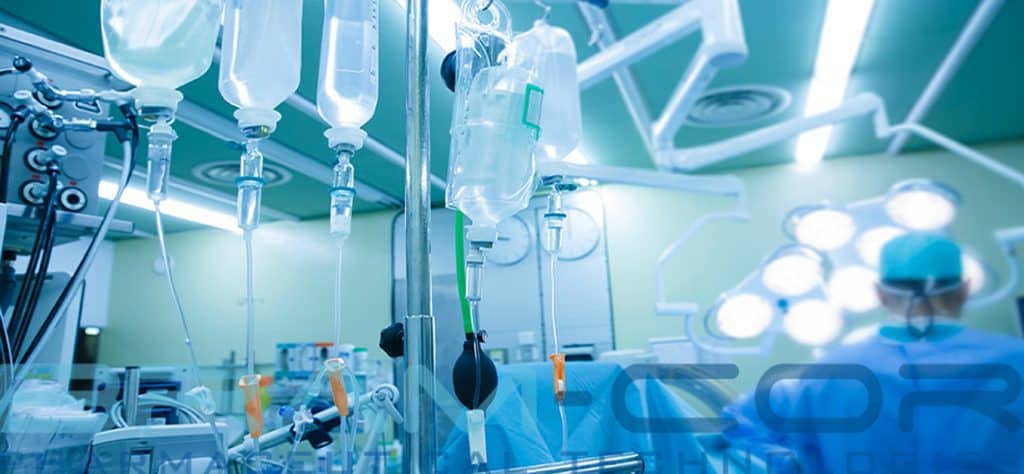
Sacche e flaconi per flebo durante un vero intervento chirurgico
Cosa significano i termini "acqua per iniettabili" e "acqua pruficata" per l'industria farmaceutica
L'acqua viene utilizzata come ingrediente e solvente in numerosi processi, formulazioni e prodotti. Pertanto, le farmacopee internazionali (USP, Ph.Eur., JP) definiscono come “acqua per preparazioni iniettabili” (WFI) solo l'acqua prevista dalle farmacopee utilizzata come eccipiente nelle soluzioni per uso parenterale.
Il Glossario ISPE distingue quindi:
- Acqua per preparazioni iniettabili bulk: «Acqua destinata alla preparazione di medicinali per somministrazione parenterale nei casi in cui l'acqua sia utilizzata come veicolo»;
- Acqua sterilizzata per preparazioni iniettabili: «(Acqua) destinata a sciogliere o diluire sostanze o preparati per somministrazione parenterale prima dell'uso».
Non-sterile medicinal products Minimum acceptable quality of water*
Vaccines for non-parenteral use (PW) Purified Water*
Oral Preparations (PW) Purified Water
Nebuliser Solutions (PW) Purified Water**
Cutaneous Preparations (PW) Purified Water***
Nasal/Ear Preparations (PW) Purified Water
Rectal/Vaginal Preparations (PW) Purified Water
Fonte: EMA/CHMP/CVMP/QWP/496873/2018. Rilasciato: 13 November 2018. Si noti che l'acqua trattata soddisfa tutti i requisiti chimici previsti per la PW (acqua purificata). Inoltre, grazie all'aggiunta del parametro relativo alle endotossine batteriche, l'acqua soddisfa i requisiti specifici della WFI. Poiché i microrganismi che tendono a proliferare nell'acqua producono endotossine, le attrezzature e le procedure utilizzate dalle linee di produzione per purificare, stoccare e distribuire la WFI devono impedire l'accumulo di endotossine e ridurre al minimo la contaminazione microbica nel sistema.
Sterile Medicinal Products Minimum acceptable quality of water*
Biologics (including vaccines and ATMP) (WFI) Water for Injection
Parenteral (WFI) Water for Injection
Ophthalmic (excluding ATMP) (PW) Purified Water
Haemofiltration Solutions / Haemodiafiltration Solutions (WFI) Water for Injection
Peritoneal Dialysis Solutions (WFI) Water for Injection
Irrigation Solutions (WFI) Water for Injection
Nasal/Ear Preparations (PW) Purified Water
Cutaneous Preparations (PW) Purified Water
Fonte: EMA/CHMP/CVMP/QWP/496873/2018. Pubblicato il 13 novembre 2018. *Si noti che l'uso di acqua per preparazioni farmaceutiche (WFI) è comunque raccomandato al fine di garantire la sicurezza dei vaccini e la qualità del prodotto. * In determinate condizioni patologiche, i medicinali devono essere sterili e apirogeni. In tali casi, è necessario utilizzare acqua per preparazioni iniettabili (WFI). ***Per alcuni prodotti, come i disinfettanti per mammelle e capezzoli ad uso veterinario, può essere consentito l'uso di acqua potabile, purché ciò sia giustificato e autorizzato.
A. ACQUA COMPENDIALE FARMACEUTICA
Gli esempi di acque compendiose in ISPE sono:
1. Acqua purificata (PW), secondo la definizione delle monografie USP / Ph.Eur.
L'acqua purificata è classificata per uso farmaceutico come eccipiente nella produzione di preparati non parenterali e, in particolare, per preparati farmaceutici, test e analisi per i quali è indicata l'acqua, salvo diversa indicazione (vedere le relative farmacopee USP, Ph.Eur. e JP come riferimento).
Pertanto, l'acqua potabile costituisce la fonte minima di acqua di alimentazione per la produzione di acqua purificata (PW), attraverso processi quali la deionizzazione, la distillazione, lo scambio ionico, l'osmosi inversa, la filtrazione o altre procedure appropriate. L'acqua purificata (PW) è inoltre una materia prima nella preparazione dell'acqua per uso farmaceutico (WFI) e del vapore puro.

Sistema di osmosi inversa Bram-Cor in una sala di trattamento dell'acqua, con serbatoio di stoccaggio dell'acqua purificata e loop dell'acqua purificata
L'acqua purificata sterile, secondo la definizione dell'USP, è acqua purificata confezionata e resa sterile; viene utilizzata in applicazioni che richiedono acqua purificata, laddove non sia possibile ricorrere a un sistema di acqua purificata convalidato (ad esempio, in caso di piccole quantità necessarie).
ACQUA PURIFICATA BULK |
||
| FISICI/CHIMICI | Ph. Eur. | |
| Aspetto Senza colore, trasparente Non definito |
||
| Conduttività | ≤ 4.3 μS/cm@20°C | |
| TOC | ≤ 0.5 mg/l | ≤ 0.50 mg/L |
| Nitrati NO₃ |
≤ 0.2 ppm | |
| MICROBIOLOGICI Ph. Eur. USP |
||
| Conta Battereologica ≤ 100 CFU/ml ≤ 100 CFU/ml |
||
| Endotossine Batteriche |
<0.25 IU/ml |
*I data potrebbero cambiare senza preavviso
2. ACQUA PER INIETTABILI (WFI) come definito dalle monografie USP / Ph.Eur.
L'acqua per preparazioni iniettabili è classificata, in ambito farmaceutico, come eccipiente nella produzione di preparati parenterali e in altri preparati farmaceutici in cui è necessario verificare il contenuto di endotossine (si vedano le farmacopee USP, EP e JP per ulteriori riferimenti).
Di conseguenza, l'acqua deionizzata (che può essere sottoposta a un pretrattamento in vista della successiva distillazione o di un processo appropriato) costituisce la fonte minima di acqua di alimentazione per la produzione di WFI. Oltre alle specifiche relative all'acqua purificata (PW), la WFI prevede l'analisi delle endotossine batteriche e soddisfa tutti i requisiti (ad eccezione dell'etichettatura) previsti per l'acqua confezionata denominata «Acqua purificata sterile» (cfr. monografia USP).
Acqua sterile per preparazioni iniettabili, secondo la definizione dell'USP. Si tratta di acqua WFI confezionata e sterilizzata; viene utilizzata in applicazioni che richiedono acqua per preparazioni iniettabili, laddove non sia possibile ricorrere a un sistema WFI convalidato (ad esempio, in caso di piccole quantità).
Acqua batteriostatica per preparazioni iniettabili, secondo la definizione dell'USP. Si tratta di acqua per preparazioni iniettabili (WFI) con l'aggiunta di uno o più conservanti antimicrobici; viene utilizzata come diluente nella preparazione di soluzioni per uso parenterale (in particolare per i prodotti multidose che consentono prelievi ripetuti).
ACQUA PER INIETTABILI BULK |
||
| FISICI/CHIMICI | Ph. Eur. | |
| Aspetto Senza colore, trasparente Non definito |
||
| Conduttività ≤ 1.1 μS/cm@20°C ≤ 1.3 μS/cm @25°C |
||
| TOC | ≤ 0.5 mg/L | ≤ 0.50 mg/L |
| Nitrati NO₃ |
≤ 0.2 ppm | |
| Alluminio ≤ 10 ppb Non definiti |
||
| MICROBIOLOGICI Ph. Eur. USP |
||
| Conta Batterica | ≤ 10 CFU/100 ml | ≤ 10 CFU/100 ml |
| Endotossine Batteriche <0.25 IU/ml |
<0.25 EU/ml |
*I data potrebbero cambiare senza preavviso

Un classico alambicco a compressione di vapore Bram-Cor STMC con un sistema di pretrattamento dell'acqua personalizzato integrato sullo stesso telaio.
La distillazione è il metodo principale per produrre WFI
Esistono due tecnologie di base che hanno segnato la storia dell'industria farmaceutica per la produzione di WFI: il sistema di distillazione a vapore compresso (VC), mediante alambicchi per la compressione del vapore, e il sistema di distillazione a multiplo effetto (ME), mediante alambicchi a più stadi.
Negli ultimi anni è diventato possibile ottenere anche WFI a freddo, da osmosi inversa.
Ciò è dovuto alle nuove generazioni di membrane che consentono l'aggiunta di una successiva fase di ultrafiltrazione (UF).
Sotto, puoi vedere nel modello CROW di BRAM-COR (Generatore WFI per osmosi inversa addizionato di un sistema di ultrafiltrazione) la coppia di filtri UF posizionati a valle.

Produrre WFI - Note sulle Farmacopee
USP 27 (2004) ha rivisto la monografia USP WFI; essa ammette WFI da "Distillazione o un processo di purificazione che è equivalente o superiore alla distillazione nella rimozione di sostanze chimiche e microrganismi".
Nel 2008 l'EMEA (European Medicines Evaluation Agency, ora EMA) ha pubblicato un documento di riflessione per spiegare perché l'uso della tecnologia a membrana non era considerato accettabile per la produzione di WFI.
Dal 2010 l'EDQM (European Directorate for Quality of Medicines & HealthCare) lavora a sondaggi per raccogliere dati industriali su "Preparazione di WFI utilizzando l'osmosi inversa (RO)".
Nel 2011 l'EDQM (Expert Workshop) ha esaminato i potenziali usi dei sistemi a membrana per la produzione di WFI e, nel 2014, ha lavorato per consentire l'inclusione delle tecnologie non di distillazione nella EP, oltre alla distillazione per la produzione di WFI.
Negli ultimi anni, i documenti (EMA Q&A EMA / INS / GMP / 489331 / 2016) e le questioni correlate vengono nuovamente esaminati.
Di conseguenza (pubblicazione EP 9.1), la monografia HPW (vedi sotto) verrà eliminata.
3. HPW (Acqua altamente purificata), come viene classificata dalla monografia Ph.Eur
(until 2018; no longer defined by Ph. Eur.)
HPW: Acqua altamente purificata (= acqua “ultra pura” industriale) è classificata dalla monografia precedente Ph.Eur. come eccipiente nella produzione di prodotti farmaceutici in cui le endotossine batteriche devono essere controllate, a meno che non sia specificato “WFI”.
4. WFH (Acqua per Emodialisi), come viene classificata dalla monografia USP
L'acqua per l'emodialisi è principalmente classificata in applicazioni farmaceutiche per l'emodialisi (vedi la relativa monografia USP), i.e. ad esempio nella diluizione di soluzioni concentrate. È prodotta da acqua potabile dell'EPA (Agenzia per la protezione ambientale degli Stati Uniti), che è stata ulteriormente purificata per ridurre i componenti chimici e microbiologici. Si noti che la WFH non è destinata all'iniezione.
Nota: l'acqua purificata (PW) o l'acqua per preparazioni iniettabili (WFI) confezionate devono essere sterilizzate per preservarne le proprietà microbiologiche; pertanto, esistono altre acque confezionate descritte nelle monografie, quali l'acqua purificata sterile, l'acqua sterile per preparazioni iniettabili, l'acqua batteriostatica per preparazioni iniettabili e così via (vedere le relative monografie dell'USP).

Produzione di soluzioni per flebo con Bram-Cor BFIL, sistema di riempimento lineare per sacche
B. ACQUE NON COMPENDIALI
Le acque non compendiali soddisfano almeno i requisiti di acqua potabile.
Si noti che le acque non compendiali non sono necessariamente di qualità inferiore rispetto alle acque compendiali. Tuttavia, i sistemi idrici non compendiali possono essere validati oppure no e, in generale, le acque non compendiali sono destinate ad avere la qualità adeguata richiesta dalla singola domanda. Per esempio: acqua potabile, acqua addolcita, acqua di ultra filtrazione, acqua di osmosi inversa, acqua EDI (processo di deionizzazione), acqua distillata.

Site sponsored by BRAM-COR Italy | waterforinjection.com Cookie Policy
USEFUL LINKS & SYSTEMS KNOWLEDGE
Main site: bram-cor.com
To view Bram-Cor Equipment catalogue
To view where Bram-Cor Equipment works
About pharmaceutical water treatment systems:
multiple-effect-water-distiller.com
vapor-compression-distiller.com
pharmaceutical-reverse-osmosis-systems.com
pure-steam-generator.com
About pharmaceutical process systems and turnkey plants:
bram-cor-pharmaprocessing.com
ivfluids-parenteralsolutions.com
pharmaceutical-turnkey.com
© 2025 BRAM-COR SPA - VIA MERCALLI 12/A - 43122 PARMA - ITALY - P.IVA 01699350342